
Principales resultados del primer trimestre para Oryzon
Añadir Estrategias de Inversión en Google
El resultado neto al cierre del primer trimestre de 2026 para Oryzon Genomics se sitúa en -1,2 M€ frente al primer trimestre del ejercicio precedente de –1,7M€, lo que supone una mejora de 0,5M€ con respecto al cierre del primer trimestre del ejercicio precedente.
Pero además, lo más significativo de sus cuentas, hasta marzo, pasa por el significativo incremento del 88% de las inversiones en I+D a 31 de marzo de 2026 en comparación al primer trimestre del ejercicio 2025. Las inversiones en I+D han ascendido a 4,5 M€, de las cuales 4,2 M€ corresponden a actividades de desarrollo y 0,3 M€ a actividades de investigación.
A 31 de marzo de 2026, Oryzon mantiene efectivo e inversiones financieras disponibles por importe de 22,1 M€. El balance a 31 de marzo de 2026 presenta un patrimonio neto de 118,3 M€.
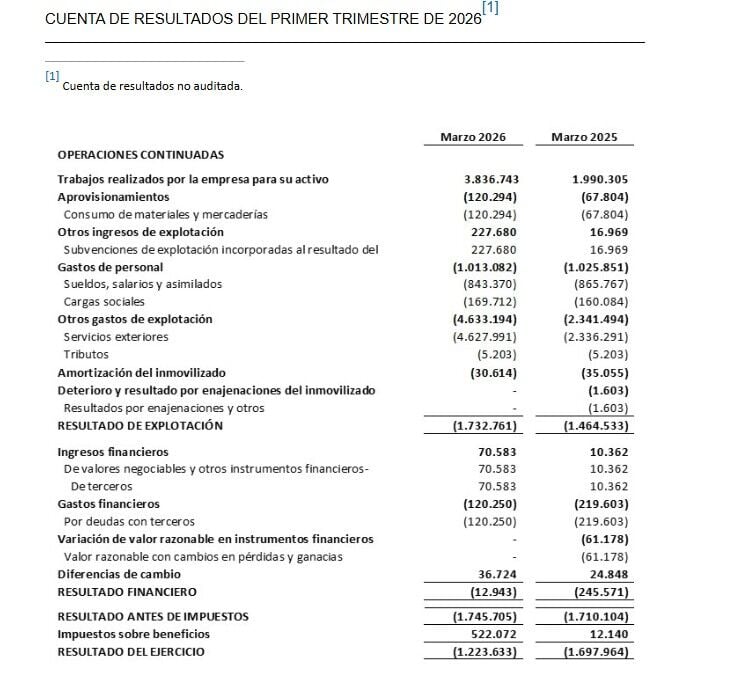
En el pasivo corriente del balance, epígrafe otros pasivos financieros, se presentan 4,1 M€, de los cuales 3,5 M€ corresponden al reconocimiento de financiación anticipada relativa a la parte de subvención IPCEI que se encuentra pendiente de ejecución, y en su caso, su importe será traspasado a patrimonio neto en el momento de su ejecución.
El Dr. Carlos Buesa, CEO de Oryzon,destaca que “durante los primeros meses de 2026, Oryzon ha seguido impulsando sus franquicias de oncología/hematología y de SNC, manteniendo al mismo tiempo una sólida posición financiera. Especialmente relevante es que iadademstat continúa generando datos clínicos muy alentadores en leucemia mieloide aguda, reforzando aún más nuestra convicción sobre el potencial terapéutico diferencial del compuesto y su oportunidad comercial.”
“Estamos especialmente entusiasmados con las próximas presentaciones en EHA 2026, donde se presentarán resultados actualizados de seguridad y eficacia de los estudios ALICE-2 y FRIDA”, ha añadido el Dr. Buesa. “En LMA de primera línea, la combinación triple de iadademstat con azacitidina y venetoclax continúa mostrando un perfil de eficacia altamente competitivo, que creemos se compara muy favorablemente con otros regímenes triples emergentes en este campo. En EHA presentaremos datos actualizados de 18 pacientes, incluyendo actividad alentadora en pacientes con perfiles genéticos adversos. Sobre la base de los avances alcanzados hasta la fecha, creemos que las combinaciones basadas en iadademstat pueden representar una oportunidad diferenciada y competitiva para un desarrollo clínico acelerado en LMA de primera línea y podrían respaldar el avance hacia un programa de Fase II/III potencialmente pivotal con el objetivo de obtener una aprobación regulatoria acelerada.”, destaca el consejero delegado de la compañía.
Evolución del negocio
Iadademstat:
Oryzon anunció la aceptación para presentación en el Congreso de la European Hematology Association (EHA) 2026 de datos positivos actualizados del ensayo clínico de Fase Ib ALICE-2 en curso con iadademstat en combinación con venetoclax y azacitidina en pacientes con leucemia mieloide aguda (LMA) de nuevo diagnóstico.
A la fecha de corte de datos para el abstract de febrero de 2026, la combinación triple continuó mostrando un perfil de seguridad favorable y elevadas tasas de respuesta. Entre los pacientes evaluables (n=14/15), la tasa de respuesta global (ORR) fue del 100% (14/14), con una tasa de respuesta completa (RC) del 79% (11/14) y una tasa de remisión completa compuesta (RCc: RC+RCh+RCi) del 93% (13/14). Tras una mediana de seguimiento de 6 meses, la tasa estimada de supervivencia global a 12 meses fue del 74%.
Datos actualizados con pacientes adicionales y respuestas más maduras serán presentados en EHA en junio de 2026. Este estudio promovido por investigadores (IIS) está liderado por el Knight Cancer Institute de Oregon Health & Science University (OHSU) y prevé reclutar hasta 24 pacientes para alcanzar 21 pacientes evaluables. El ensayo continúa reclutando pacientes activamente.
Vafidemstat:
Oryzon continúa con las actividades regulatorias y de desarrollo necesarias para respaldar el avance del ensayo PORTICO-2 de Fase III con vafidemstat en agresividad en trastorno límite de la personalidad (TLP).
Tras la recepción de comentarios por escrito de la FDA relativos a los criterios de valoración del estudio y a determinadas consideraciones no clínicas, la Compañía está trabajando activamente en la generación de información adicional de soporte y en el refinamiento del protocolo requeridos para su nueva presentación. Estas actividades incluyen investigación cualitativa y trabajos de validación de criterios de valoración destinados a reforzar las escalas clínicas propuestas.

